
3.2 反應活性
3.2.1 基質結構的影響
(1)定位效應
在按SNAr2歷程進行的芳香族親核取代反應里,吸電子基團引導進入基團定位在鄰位和對位。相似地,在Ar-X中,CF3,Cl,Br,I,SMe等主要是對位定位,NH2和O-是間位定位。
但是在絕大多數地芳香族親核取代反應中,在分子中只有一個即將離去的離去基團,因而研究的注意力并不主要集中在定位效應上。
在通過苯炔中間體進行的反應中,有兩個因素影響進入基團的位置。首先是苯炔生成的方向。當取代基在離去基團的鄰位或對位時沒有選擇:
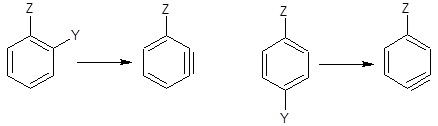
但是,有一個間位基團時,則苯炔可以通過兩個不同的途徑形成:
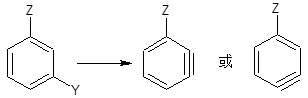
在這種情況下,總是脫掉酸性比較強的氫。
第二個因素是形成的苯炔有兩個位置可以被進攻。有利于親核試劑進攻的位置是導致形成比較穩定的碳負離子中間體的位置。
(2)反應活性
吸電子取代基對按SNAr2歷程進行的反應有致活作用,特別是在即將離去的基團的鄰位和對位的吸電子取代基的致和作用更大,而給電子取代基則有致鈍作用。這種情況和在芳香族親電取代反應里的恰好相反。
芳香環里的雜氮原子也有強的致活作用,成為季胺離子后,作用更大。研究SNAr2歷程最常使用的基團是硝基。苯環沒有活化基團,不適用于研究SNAr2歷程。
3.2.2 離去基團的效應
在芳香族親核取代反應中,不僅鹵素、硫酸根、磺酸基、NR3+可以作為離去基團,而且NO2、OR、OAr、SO2R和SR等也可以作為離去基團。尤其是,硝基是一個特別好的離去基團。離去基團的活潑性順序可以大致排列為:F>NO2>OTs>SOPh>Cl,Br,I>N3>NR3+>OAr,OR,SR,SO2R,NH2。但是,這種次序主要還要看親核試劑的性質。在鹵素中,氟是比較好的離去基團。其它的鹵素活性都很接近,它們的次序一般是Cl>Br>I,但并非永遠如此。在SNAr2歷程中的離去基團的次序和在SN1歷程和SN2歷程中的很不相同。這種情況似乎是由于SNAr2歷程的第一步反應通常是速率決定步驟,而這步反應被強的吸電子的(具有強的—I效應的)基團所促進的,因而,在SNAr2歷程里,-I效應很強的基團(如Cl和NO2)比較容易被置換。另外一種解釋是說氟是在鹵素中唯一容易形成氫鍵的,它和親核試劑形成氫鍵,因而是一個比較好的離去基團。自然,只有在親核試劑中有氫時才有這種可能。在反應的第二步是速度決定步驟的SNAr2歷程中,和在苯炔歷程中,氟是鹵素中最壞的離去基團。SN1歷程中,只有N2+是重要的離去基團。
3.2.3 進攻的親核試劑的效應
不同的作用物和不同的反應條件將導致不同的親核性次序,因而不可能建立一個不變的親核性次序,但是一個總的大致次序是:NH2->Ph3C->PhNH—(芳香炔歷程)>ArS->RO->R2NH>ArO->OH->ArNH2>NH3>I->Br->Cl->H2O>ROH。和脂肪族親核取代反應一樣,親核性和堿性強度有關。當進攻的原子是周期表中同族的原子時,它們的親核性依據它們在周期表中的位置由上而下的順序遞增。但是,也有例外;例如:OH-的堿性比ArO-的強,但是它是一個比較差的親核試劑。在一系列相似的親核試劑(如取代苯胺)中,親核性是和堿性相互關聯的。奇怪的是除個別情況外,氰負離子不能作為親核試劑取代在芳香體系上。
4 說明
本文由參考文獻1-2相關章節縮寫而成。
參考文獻
[1] [美] J.馬奇著陶慎熹趙景旻譯《高等有機化學》,人民教育出版社,1982.
[2] 高振衡編《物理有機化學》,高等教育出版社,1983.




